


Рассмотрим ответы на Вопросы к параграфу 43 из учебника по химии для 9 класса Рудзитиса
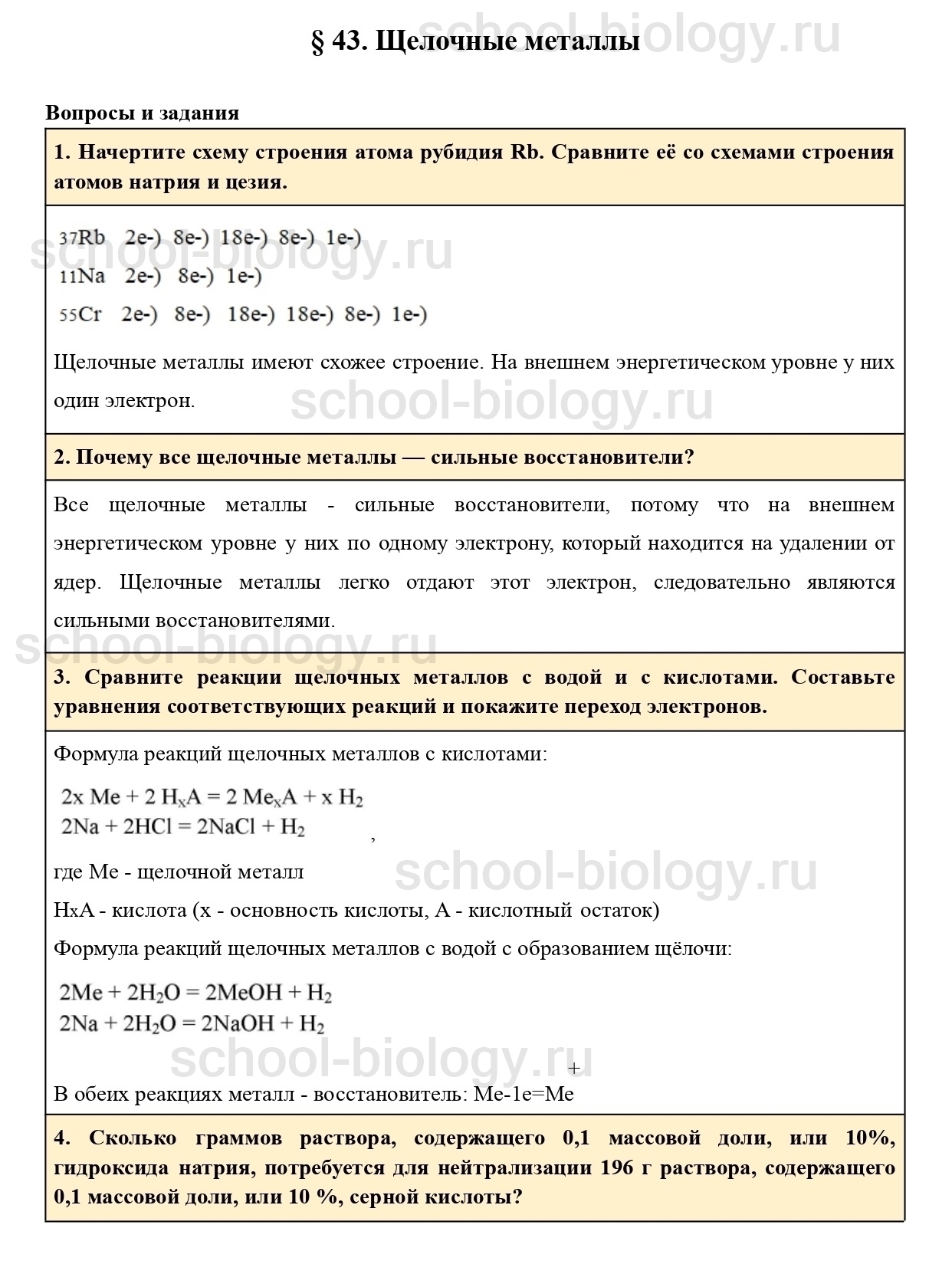
1. Начертите схему строения атома рубидия Rb. Сравните её со схемами строения атомов натрия и цезия.
2. Почему все щелочные металлы — сильные восстановители?
3. Сравните реакции щелочных металлов с водой и с кислотами. Составьте уравнения соответствующих реакций и покажите переход электронов.
4. Сколько граммов раствора, содержащего 0,1 массовой доли, или 10%, гидроксида натрия, потребуется для нейтрализации 196 г раствора, содержащего 0,1 массовой доли, или 10 %, серной кислоты?
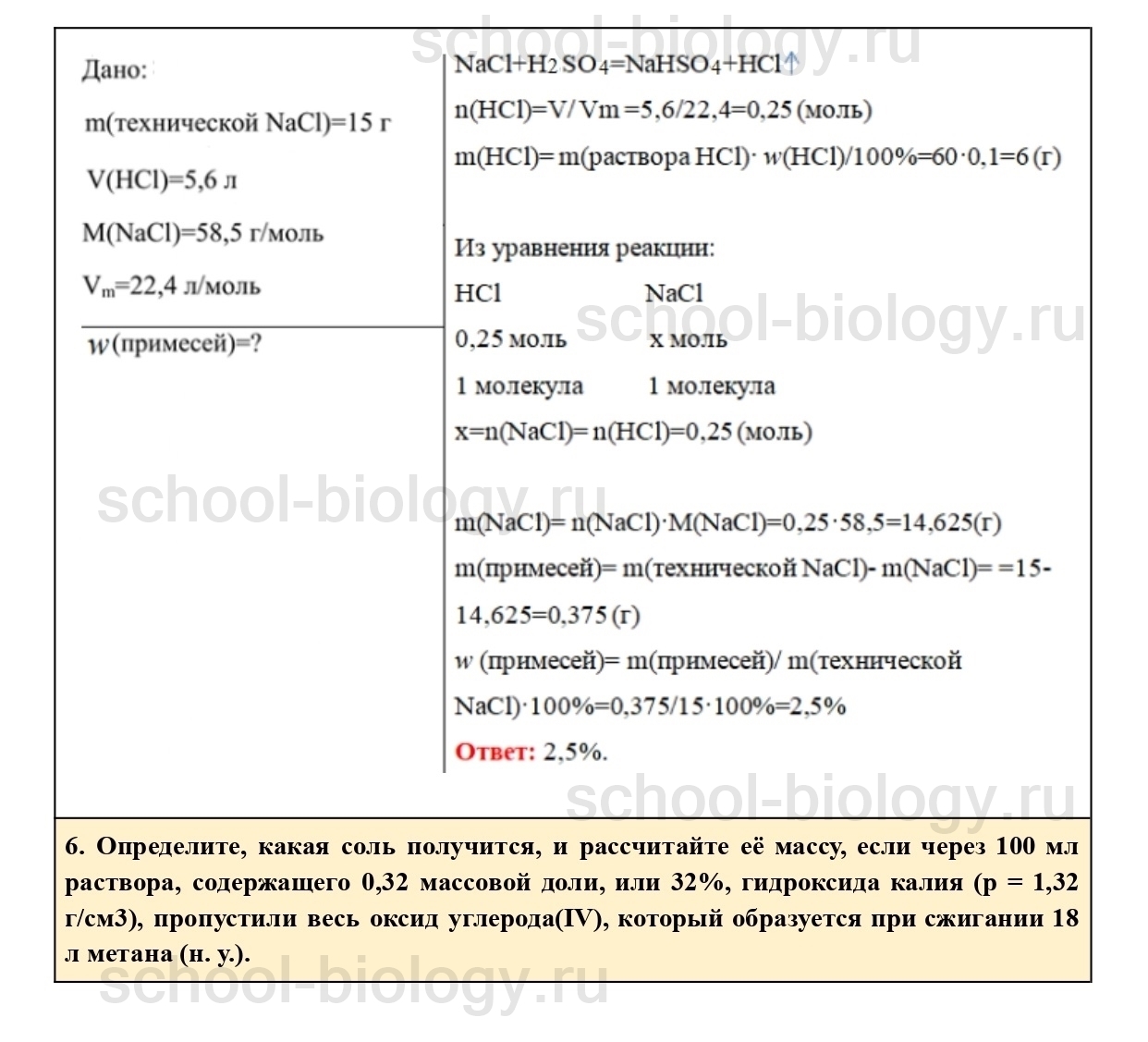
5. При обработке 15 г технической поваренной соли концентрированной серной кислотой выделилось 5,6 л газа (н. у.). Рассчитайте массовую долю (в процентах) примесей в поваренной соли.
6. Определите, какая соль получится, и рассчитайте её массу, если через 100 мл раствора, содержащего 0,32 массовой доли, или 32%, гидроксида калия (р = 1,32 г/см3), пропустили весь оксид углерода(IV), который образуется при сжигании 18 л метана (н. у.).
1. Химический элемент, атомная масса которого 23, а число нейтронов в ядре равно 12, в периодической системе находится
1) в 3-м периоде, IБ-группе
2) в 4-м периоде, IIIА-группе
3) в 4-м периоде, VIIБ-группе
4) в 3-м периоде, IA-группе
2. При взаимодействии калия с водой наряду с водородом образуется
1) оксид
2) гидроксид
3) пероксид
4) гидрид
3. Необходимо строго соблюдать правила безопасности, работая веществом
1) КСl
2) КОН
3) Сu
4) NaCl
1. Начертите схему строения атома рубидия Rb. Сравните её со схемами строения атомов натрия и цезия.
2. Почему все щелочные металлы — сильные восстановители?
3. Сравните реакции щелочных металлов с водой и с кислотами. Составьте уравнения соответствующих реакций и покажите переход электронов.
4. Сколько граммов раствора, содержащего 0,1 массовой доли, или 10%, гидроксида натрия, потребуется для нейтрализации 196 г раствора, содержащего 0,1 массовой доли, или 10 %, серной кислоты?
5. При обработке 15 г технической поваренной соли концентрированной серной кислотой выделилось 5,6 л газа (н. у.). Рассчитайте массовую долю (в процентах) примесей в поваренной соли.
6. Определите, какая соль получится, и рассчитайте её массу, если через 100 мл раствора, содержащего 0,32 массовой доли, или 32%, гидроксида калия (р = 1,32 г/см3), пропустили весь оксид углерода(IV), который образуется при сжигании 18 л метана (н. у.).
1. Химический элемент, атомная масса которого 23, а число нейтронов в ядре равно 12, в периодической системе находится
1) в 3-м периоде, IБ-группе
2) в 4-м периоде, IIIА-группе
3) в 4-м периоде, VIIБ-группе
4) в 3-м периоде, IA-группе
2. При взаимодействии калия с водой наряду с водородом образуется
1) оксид
2) гидроксид
3) пероксид
4) гидрид
3. Необходимо строго соблюдать правила безопасности, работая веществом
1) КСl
2) КОН
3) Сu
4) NaCl
